ÁTOMO
Los átomos son la unidad básica de toda la materia, la estructura que define a todos los elementos y tiene propiedades químicas bien definidas. Todos los elementos químicos de la tabla periódica están compuestos por átomos con exactamente la misma estructura.
Resumen del vídeo.- Todo lo que nos rodea contiene átomos, como un grano de arena que contiene trillones de átomos,principal componente de la materia.
Sus principales componentes son: Núcleo,Protones,Neutrones y Electrones.

Núcleo.- Es el centro del átomo, es la parte más pequeña del átomo y allí se conservan todas sus propiedades químicas. Casi que toda la masa del átomo reside en el núcleo.
Protones.- Son uno de los tipos de partículas que se encuentran en el núcleo de un átomo y tienen carga positiva (masa = 1.673 x 10-24 gramos).
Neutrones.- Los neutrones son partículas ubicadas en el núcleo y tienen una carga neutra (masa = 1.675 x 10-24 gramos).
Electrones.- Éstas son las partículas que orbitan alrededor del núcleo de un átomo, tienen carga negativa y son atraídos eléctricamente a los protones de carga positiva (masa = 9.10 x 10-28 gramos).
CLASES DE ÁTOMOS
Es la porción mínima de un elemento químico que al ser combinado con otros puede construir moléculas.

HIDROGENOIDES
Son tipos de átomos compuestos por un solo electrón y un núcleo.
Es isoelectrónico en cuanto al átomo de hidrógeno, lo cual le otorga
un parecido comportamiento, varios de los exóticos también
cuentan con un comportamiento hidrogenoide.
El hidrógeno cuenta con isótopos, cualquiera de ellos es hidrogenoide.
INTERSTICIALES
Los átomos intersticiales derivan de la acción de uno suplementario que en un mineral se ubica en su red cristalina provocando la distorsión del átomo. Este fenómeno puede ser forzado con la irradiación del cristal para otorgarle energía.
EXÓTICO
Es análogo a uno normal con una o más cantidad de partículas que son reemplazadas por las elementales distintas.
MODELOS ATÓMICOS
Un modelo atómico es una representación estructural de un átomo,que trata de explicar su comportamiento y propiedades. A lo largo del tiempo existieron varios modelos atómicos y algunos más elaborados que otros.
 Modelo Atómico de Democrito.- (450 a. C.), el primer modelo atómico, postulado por el filósofo griego Demócrito. Esta era considerada como indivisible e indestructible, se la llamaba la partícula más pequeña de la materia. Modelo Atómico de Dalton.- (1803), que surgió en el contexto de la química, el primer con bases cientificas
Modelo Atómico de Democrito.- (450 a. C.), el primer modelo atómico, postulado por el filósofo griego Demócrito. Esta era considerada como indivisible e indestructible, se la llamaba la partícula más pequeña de la materia. Modelo Atómico de Dalton.- (1803), que surgió en el contexto de la química, el primer con bases cientificas
Modelo Atómico de Thomson.- (1904), o modelo del pudin, donde los electrones son como las "frutas" dentro de la "masa" positiva.
Modelo Atómico de Rotherford.- (1911), el primero que distingue entre el núcleo central y una nube de electrones a su alrededor.
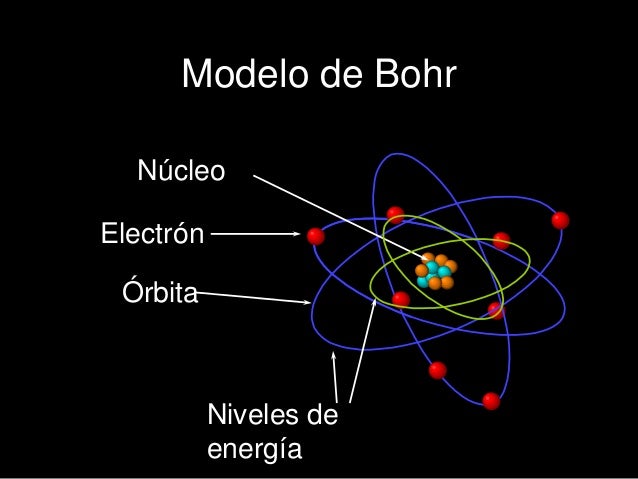
Modelo Atómico de Bohr.- (1913) en el que los electrones giraban en órbitas circulares.
Modelo Atómico de Sommerfeld.- (1916), una versión relativista del modelo de Rutherford-Bohr.
Modelo Atómico de Schrodinger.- (1926), un modelo cuántico no relativista donde los electrones se consideran ondas de materia existente. Este modelo es el que sigue actualmente.
Espero les sirva y sea de su agrado